摘要:盡管干細胞療法在歷年來的發展日新月異,但安全性、倫理性和監管始終是保障患者安全的關鍵。了解干細胞、細胞療法或間充質干細胞的倫理獲取、開發和監管方式,將有助于患者做出明智的選擇。
干細胞療法已從抽象概念走向現實應用,為關節退行性疾病、自身免疫性疾病等患者提供了長期治愈的可能,而不僅僅是緩解癥狀。然而,隨著全球干細胞臨床轉化的加速,安全性爭議、倫理困境以及監管政策的“松緊帶”效應,正成為2026年患者必須正視的新課題。
因此,到了2026年,患者不再僅僅問“它有效嗎?”,他們還會問“它安全、合乎倫理且科學可靠嗎? ”。本文章將結合2026年最新的國內外政策與真實案例,指導患者了解他們需要知道的有關干細胞和細胞療法的安全性、倫理和監管方面的信息。
一、了解干細胞治療中安全的重要性:從“實驗室標準”到“真實世界證據”
在進行任何細胞療法(包括干細胞療法)時,安全性是成功進行再生治療的基礎,并且取決于幾個受控的臨床因素:
- 對間充質干細胞(MSCs)進行適當的篩選和鑒定,以確保其活力、純度和再生潛能。
- 受控的實驗室處理流程,以防止污染并維持無菌條件。
- 精準給藥和靶向給藥方法可減少不良反應并提高治療效果。
- 根據病史仔細篩選患者,以避免不適宜或高風險的應用。
2026年政策與案例洞察:
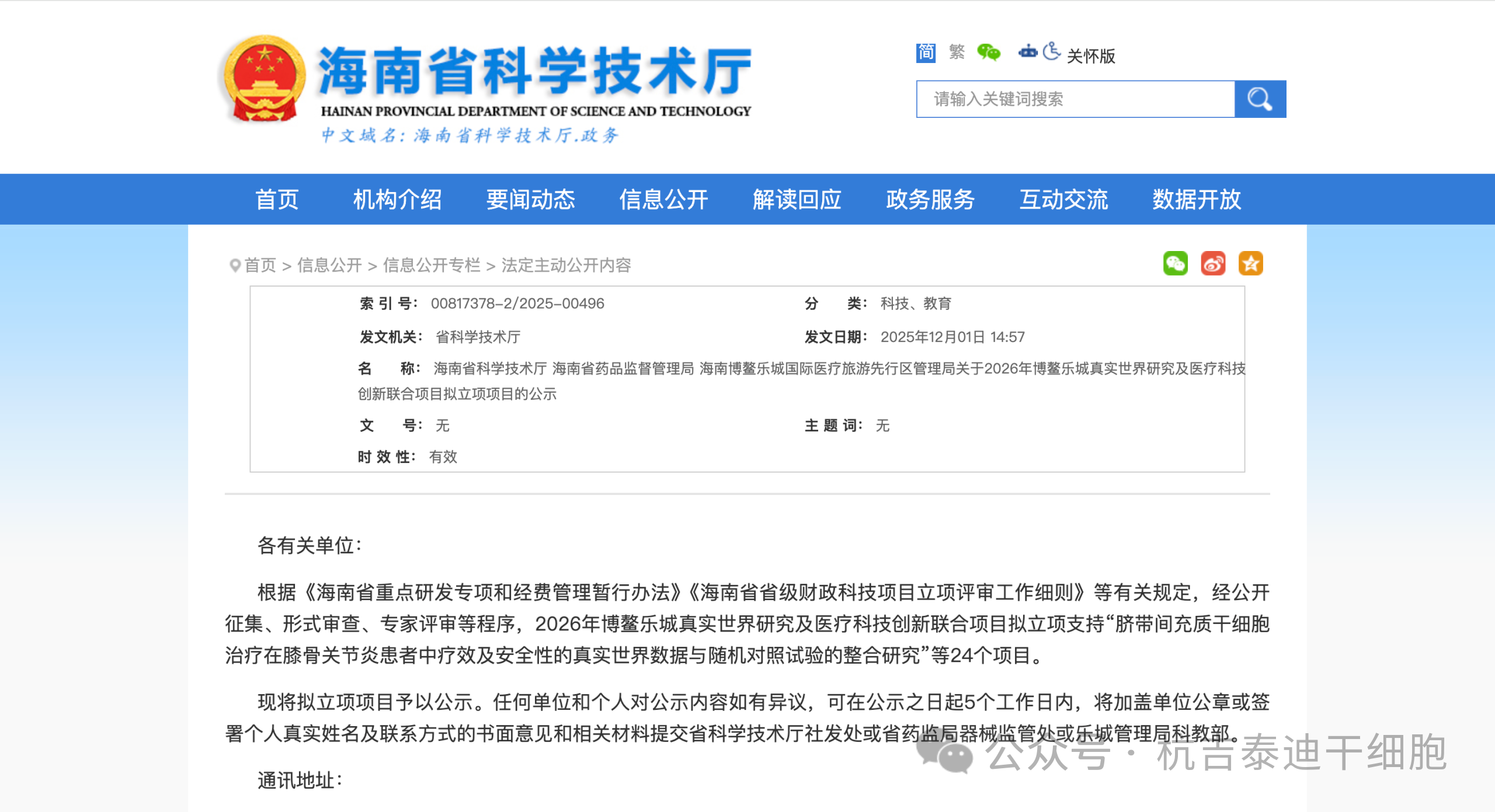
安全性驗證正在從“理論要求”走向“真實世界數據強制收集”。2026年初,海南博鰲樂城正式將“臍帶間充質干細胞治療膝骨關節炎”納入真實世界研究項目,這意味著干細胞療法的有效性不再僅依賴小規模臨床試驗,而是必須在實際臨床應用中接受持續性監測。
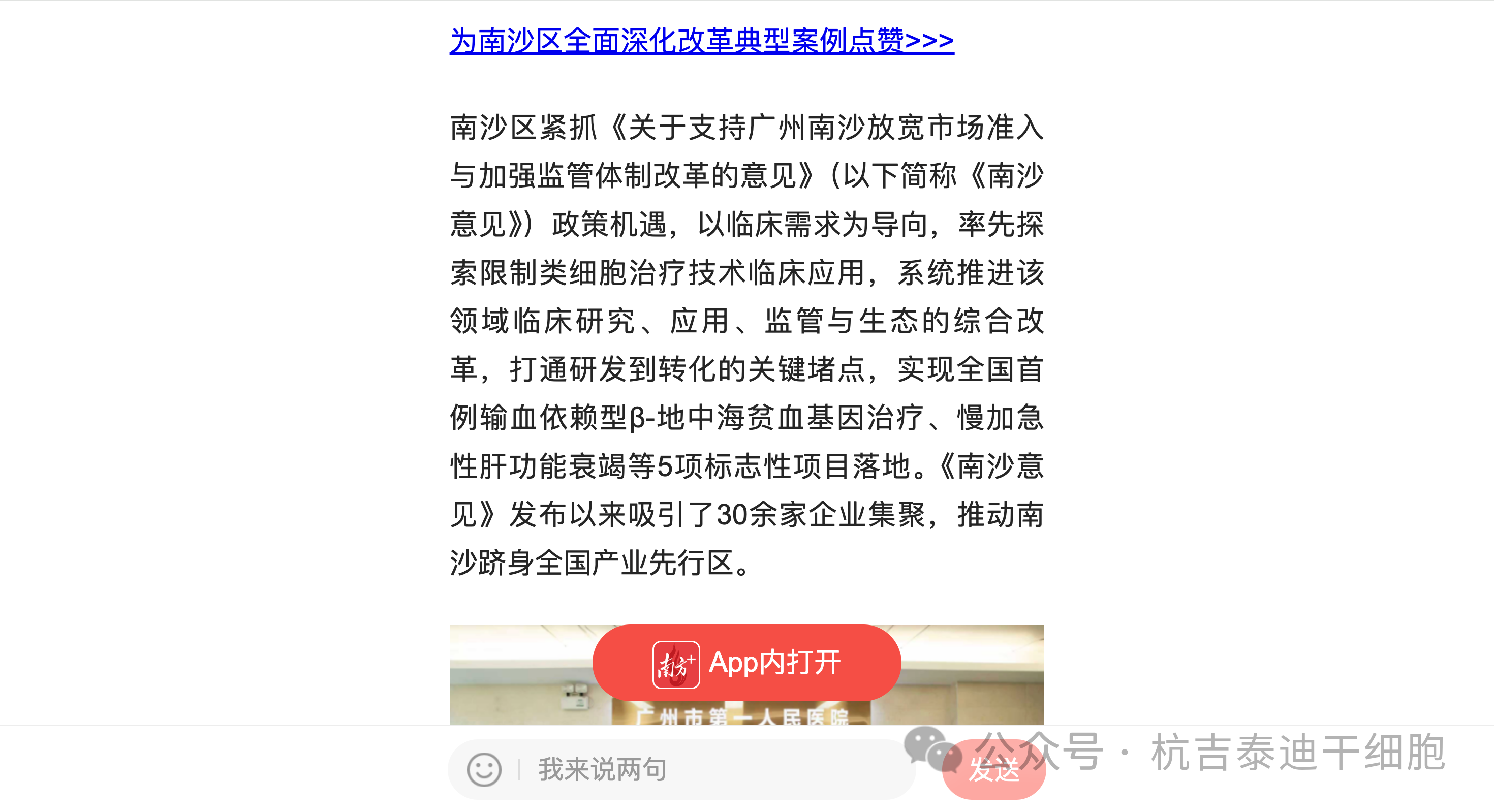
同期,廣州南沙完成了全國首例輸血依賴型β-地中海貧血基因治療及異體干細胞治療肝衰竭,72例地貧治療患者中已有31例徹底脫離輸血依賴。這些突破的背后,是嚴格的患者篩查、無菌制備及長期隨訪體系在支撐——這正是安全落地的關鍵。
反面警示:
安全并非天然伴隨新技術而來。日本“快速審批”框架下的脊髓損傷療法Stemirac,2024年因同類產品HeartSheet在確證性試驗中顯示治療組死亡風險是對照組的1.9倍而被撤銷批準,Stemirac自身也面臨2025年底能否通過確證試驗的生死關。這一案例向2026年的患者發出明確信號:僅憑“政府批準”或“已上市”不足以判斷安全,必須核實是否有強制性的長期隨訪數據。
現代再生醫學強調最大限度地減少免疫反應、感染風險和不可預測的后果。到2026年,安全規程正通過真實世界證據體系實現標準化與個體化的平衡。
二、為什么我們需要細胞療法的倫理基礎?從“獲取透明”到“政策博弈”
倫理規范確保再生醫學以患者利益為導向,不會辜負患者的希望。干細胞療法的倫理遵循以下準則:
- 透明且自愿的捐贈者同意。
- 以合乎倫理的方式,在不使用武力的情況下獲取干細胞。
- 溝通中的誠實在于權衡利弊。
- 遠離毫無根據和未經證實的說法。
間充質干細胞因其再生特性而被廣泛應用,且在來源(如臍帶、胎盤)與應用方式合理的情況下,倫理問題相對較少。然而,2026年的倫理語境已發生重要變化。
2026年倫理爭議焦點:
2026年1月,美國國立衛生研究院(NIH)突然頒布新政,終止對“人胎兒組織研究”的聯邦資金支持。國際干細胞研究學會(ISSCR)立即發表聲明反對,指出胎兒組織來源的細胞系在過去一個世紀中對疫苗開發、神經退行性疾病研究至關重要,且此類研究長期受嚴格的倫理框架(知情同意、非營利性捐贈)約束。

這一事件向患者揭示了一個深層事實:干細胞的“倫理安全”不僅取決于來源本身,還受到公共衛生
政策波動的影響。當某種干細胞來源突然被政治或法規切斷,依賴該來源的在研療法可能面臨中斷風險。
來自臨床一線的倫理實踐:
2026年1月,海南博鰲樂城完成了首例類風濕關節炎臍帶間充質干細胞治療。該技術此前已完成三期臨床試驗,且單次治療費用僅為美國同類療法的1/5,通過“按療效付費”等創新支付模式減輕患者負擔。合乎倫理的實踐不僅關乎“細胞怎么來”,更關乎患者是否因經濟門檻被排除在創新療法之外。

符合倫理的實踐能夠保護患者免受誤導性治療,并建立人們對細胞療法的信任。
三、干細胞治療的監管:全球化協調與“區域性試驗田”
監管的作用在于區分循證醫學和高風險實驗。監管框架的主要關注領域包括:
- 干細胞處理的質量控制
- 治療方案的記錄
- 臨床隨訪和結果監測
- 符合生物醫學安全標準
2026年監管格局新特征:
全球范圍內的監管協調程度有所提高,但呈現出 “成熟市場收緊、亞洲先行區試點突破” 的分化態勢。
中國的“先行先試”經驗:
- 海南博鰲樂城:依托“特許醫療”政策,2026年已密集落地類風濕關節炎干細胞治療、膝骨關節炎真實世界研究等項目。其核心價值在于:將審批周期從數年壓縮至數月,同時強制要求真實世界數據收集,為全國監管政策提供“沙盒實驗”樣本。
- 廣州南沙:率先探索限制類細胞治療技術臨床應用,構建區域臨床應用項目審查機制,已落地5項標志性項目。
- 北京昌平:2026年1月在愛爾蘭總理見證下,引進愛爾蘭奧森干細胞公司,加速糖尿病并發癥治療管線的本土化臨床試驗。昌平區在研管線達190余條,占全國IND批件的5%。
國際監管的“日本教訓”:
日本的條件性限時批準制度允許基于小樣本、非對照數據上市,導致Stemirac等產品陷入“批準了卻證不明確有效”的尷尬境地。2026年,這一模式的警示意義被全球引為監管過度寬松的反面教材。
四、為什么監管對患者至關重要?(附2026年決策指南)
監管在保護接受干細胞治療和其他細胞療法的患者方面發揮著至關重要的作用。以下是監管如何直接惠及患者:
1. 持續的治療質量
監管確保干細胞的獲取、處理、儲存和輸送流程標準化。2026年案例:美國FDA近期批準了Cabaletta Bio公司的CAR-T自體療法在全自動封閉平臺上生產,這正是通過生產流程的標準化來降低批次差異。
2. 降低感染或排異風險
嚴格的監管規程要求實驗室環境必須無菌,并進行污染檢測和患者篩查。2026年案例:廣州南沙的干細胞移植治療中心配備了30間層流病房、150張床位,物理環境本身就是監管合規性的體現。
3. 基于研究的適應癥限制
監管框架將間充質干細胞的用途限制在有科學證據支持的適應癥范圍內。2026年案例:馬來西亞一項針對哮喘、COPD患者的霧化吸入外泌體治療研究顯示,三名患者在GMP級生產條件下接受治療,肺功能指標(FEV1/FVC)顯著改善,且未出現任何嚴重不良事件——這正是研究與臨床界限清晰的范例。

4. 長期患者安全監測
受監管的干細胞療法需要結構化的隨訪和療效監測。2026年趨勢:無論是海南的真實世界研究,還是日本的Stemirac確證試驗,監管機構都在強制要求可追溯的結局數據。患者有權要求治療機構出示同類適應癥的隨訪數據。
五、結語
到2026年,干細胞療法的未來已不再是抽象的理論探討。海南的真實世界數據、南沙的地貧治愈案例、日本的監管受挫、美國的倫理政策逆轉——所有這些正在發生的事件共同塑造了干細胞療法的真實面貌。
對于患者而言,2026年的核心問題是:你所接受的療法,是否處于“負責任的政策試驗田”之中,還是在監管真空地帶游走?
通過合理運用干細胞、間充質干細胞和細胞療法,患者將能夠獲得創新且可靠的再生治療。
常見問題(2026年2月更新)
Q1:2026年干細胞療法是否安全?
答:取決于“在哪里做”以及“是否有真實世界數據支撐”。博鰲樂城、廣州南沙等監管試點區因強制要求數據收集和質量控制,安全更有保障;而純粹以商業推廣為目的、拒絕提供既往同類患者隨訪數據的機構,風險極高。
Q2:間充質干細胞主要用于什么用途?
答:當前最成熟的循證應用集中在膝骨關節炎、類風濕關節炎、肝纖維化、糖尿病并發癥、神經系統損傷等領域。其優勢在于免疫原性低、倫理爭議小。
Q3:所有干細胞療法都受到監管嗎?
答:并非所有療法都受到同等監管。患者應核實治療是否遵循國家或國際認可的臨床和倫理準則,以及是否在國家藥品監管部門(如國家藥監局、海南省衛健委、樂城管理局)有備案記錄。
Q4:患者可以通過哪些途徑找到符合倫理的干細胞來源?
答:有道德的供應商會明確告知細胞來源組織(臍帶/胎盤/脂肪等)、制備機構是否通過GMP認證、是否經過無菌及支原體檢測,并會主動提供客觀的風險說明,而非只展示成功案例。
Q5:法規是否會影響干細胞療法的獲取?
答:監管既可能通過“特許政策”加速合法療法的可及性(如海南、南沙模式),也可能因倫理政策突變導致某些療法供應鏈中斷(如NIH胎兒組織禁令)。患者應關注政策動態,避免選擇依賴單一爭議來源的療法。
參考資料:
[1]:Hyun I., 2010 – The bioethics of stem cell research and therapy
Explains ethical principles, informed consent, and patient protection in stem cell research and clinical use.https://pmc.ncbi.nlm.nih.gov/articles/PMC2913594/
[2]:Trounson A., McDonald C., 2015 – Stem cell therapies in clinical trials: Progress and challenges.Supports regulatory oversight, clinical safety requirements, and ethical challenges in translating stem cell therapy to practice.https://www.nature.com/articles/nrm.2015.10
[3]:Galipeau J., Sensébé L., 2018 – Mesenchymal stromal cells: Clinical challenges and therapeutic opportunities
Details safety considerations, immune modulation, and regulated clinical use of mesenchymal stem cells.https://www.sciencedirect.com/science/article/pii/S1525001625000930
[4]:Taylor C.J. et al., 2018 – Regulatory issues in stem cell research and therapy
Discusses international regulatory frameworks, quality control, and patient safety monitoring in stem cell therapies.https://pmc.ncbi.nlm.nih.gov/articles/PMC6029272/
[5]:Marks P., Witten C., Califf R., 2017 – Clarifying stem-cell therapy regulation
Explains how regulatory agencies distinguish evidence-based stem cell therapies from unsafe or unproven interventions.https://www.nejm.org/doi/full/10.1056/NEJMp1701469
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。



 掃碼添加官方微信
掃碼添加官方微信