2026年3月1日,《Diabetes & Metabolism》發(fā)表題為“干細(xì)胞治療糖尿病的主要臨床試驗(yàn)概述”的研究綜述[1]。文章指出,基于干細(xì)胞的療法正引領(lǐng)糖尿病治療從癥狀控制邁向病因干預(yù),其核心目標(biāo)在于恢復(fù)胰島素分泌細(xì)胞的功能。干細(xì)胞療法重塑糖尿病治療格局已實(shí)現(xiàn)從供體胰島移植(如埃德蒙頓方案)向人多能干細(xì)胞來源的β細(xì)胞替代療法的關(guān)鍵跨越。

干細(xì)胞療法重塑糖尿病治療格局——主要臨床試驗(yàn)概述與未來展望
一、全球健康挑戰(zhàn)與治療困境
糖尿病是21世紀(jì)最緊迫的全球性健康挑戰(zhàn)之一。患者規(guī)模持續(xù)攀升,預(yù)計(jì)到2025年將影響全球8.3億人,給各國醫(yī)療系統(tǒng)帶來沉重負(fù)擔(dān)。盡管藥物研發(fā)、胰島素輸注技術(shù)與血糖監(jiān)測手段長足進(jìn)步,但現(xiàn)有治療策略本質(zhì)上仍屬姑息性,無法實(shí)現(xiàn)根治。
1型糖尿病患者需終身依賴外源性胰島素;2型糖尿病則面臨進(jìn)行性β細(xì)胞功能障礙與胰島素抵抗的雙重困境。這些局限凸顯了開發(fā)再生療法的緊迫性——恢復(fù)內(nèi)源性胰島素分泌,實(shí)現(xiàn)持久穩(wěn)態(tài)的血糖控制,從根本上變革現(xiàn)有治療范式。
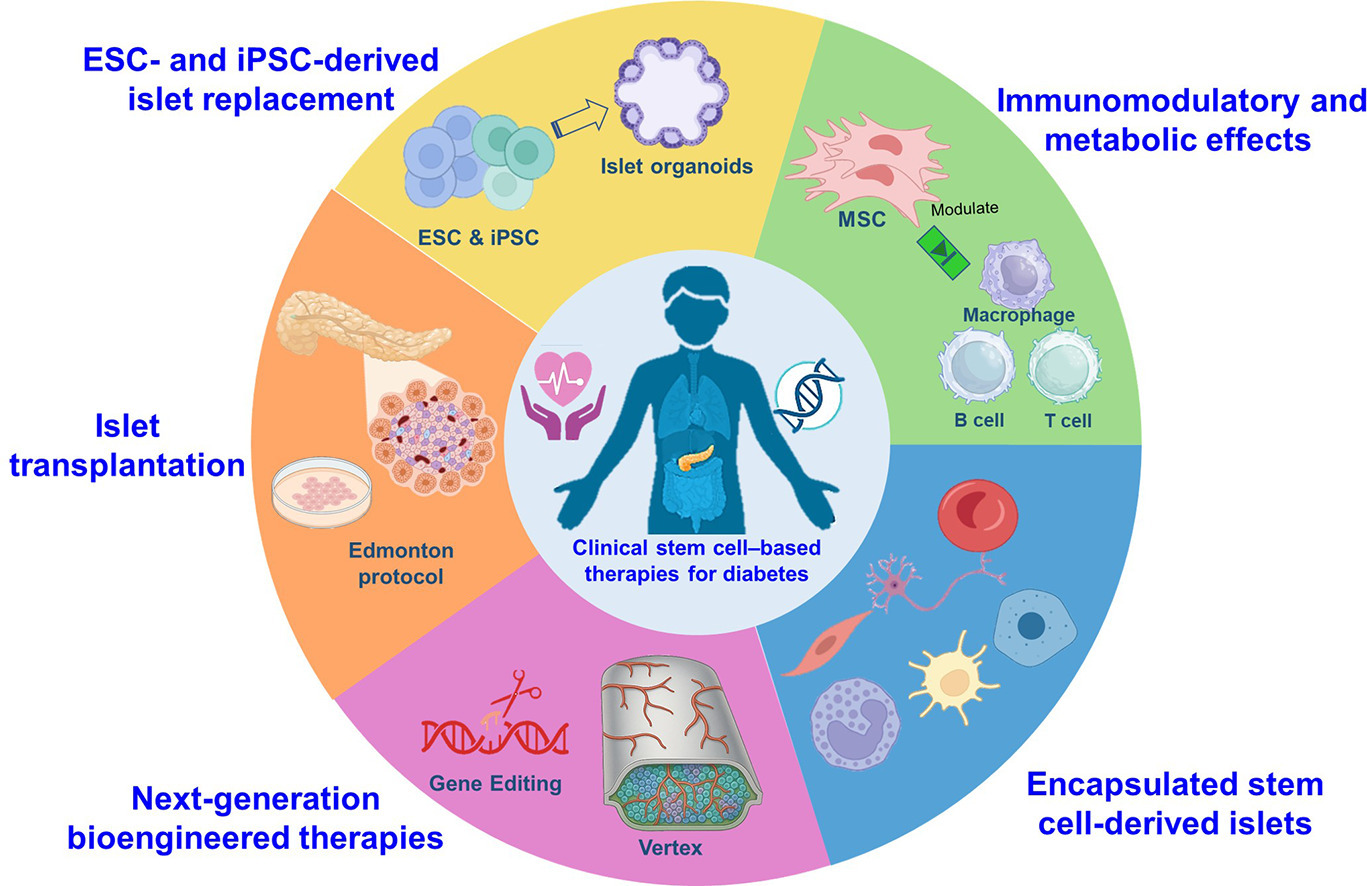
二、理論基礎(chǔ)與臨床前證據(jù)
在此背景下,基于人類多能干細(xì)胞(包括胚胎干細(xì)胞和誘導(dǎo)多能干細(xì)胞)及間充質(zhì)干細(xì)胞的療法應(yīng)運(yùn)而生,成為最具前景的再生策略。這些干細(xì)胞具備分化為胰島素分泌細(xì)胞或調(diào)節(jié)免疫代謝通路的獨(dú)特能力,有望為糖尿病治療帶來范式轉(zhuǎn)變(圖1)。
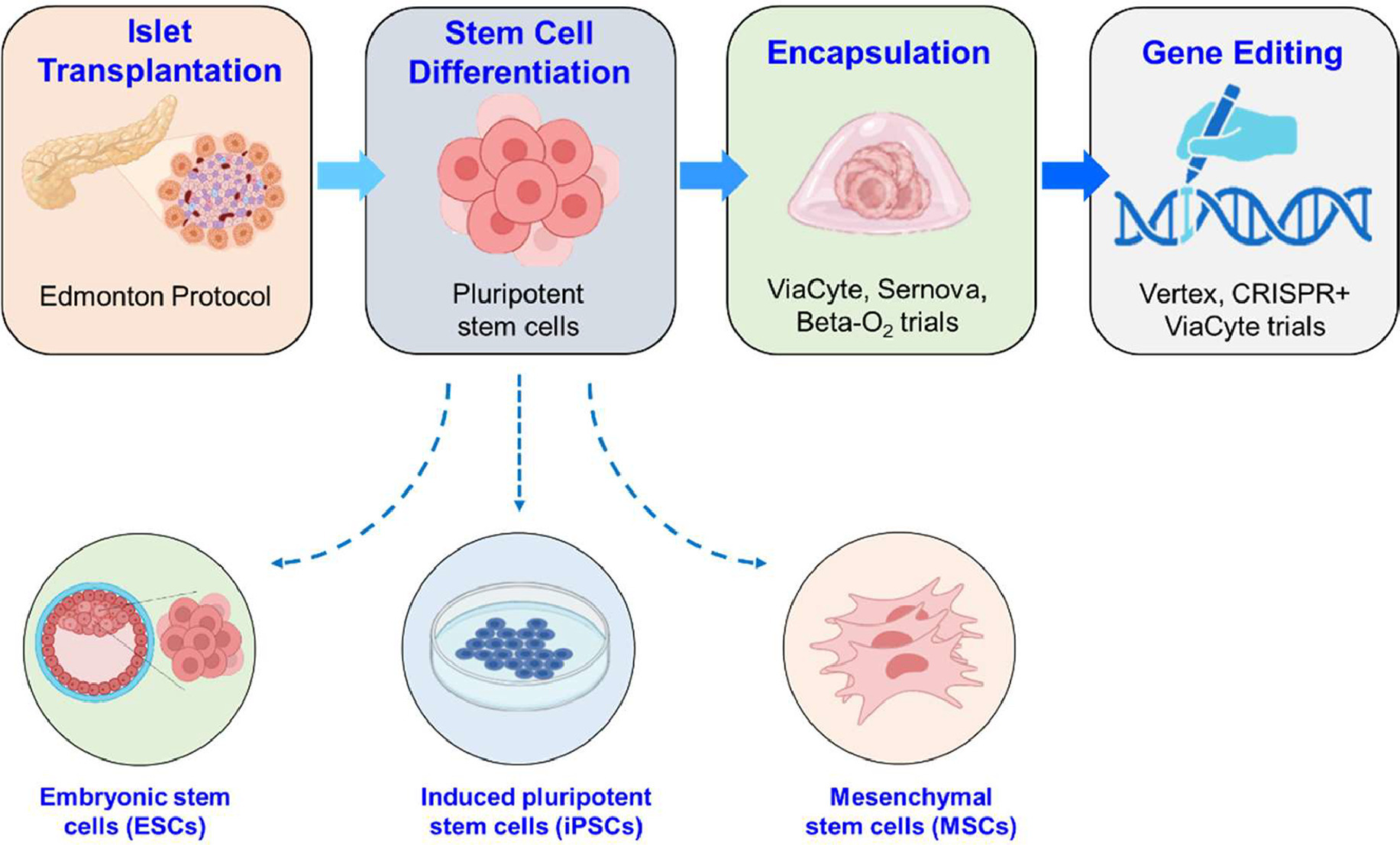
臨床前研究證實(shí),通過定向分化技術(shù)可引導(dǎo)多能干細(xì)胞和胰腺祖細(xì)胞生成能響應(yīng)葡萄糖刺激并分泌胰島素的β樣細(xì)胞。同時(shí),間充質(zhì)干細(xì)胞憑借其免疫調(diào)節(jié)與抗炎特性,展現(xiàn)出保護(hù)1型糖尿病患者殘余β細(xì)胞功能、改善2型糖尿病胰島素敏感性的潛力。
三、從實(shí)驗(yàn)室到臨床:干細(xì)胞療法的里程碑式轉(zhuǎn)化
過去二十年間,這些臨床前研究的突破已成功轉(zhuǎn)化為日益增多的臨床試驗(yàn)。具有里程碑意義的埃德蒙頓胰島移植方案驗(yàn)證了β細(xì)胞替代療法的可行性,但其廣泛應(yīng)用受限于供體短缺和免疫排斥(表1)。
| 干細(xì)胞 | 起源 | 分化潛能 | 優(yōu)勢 | 局限性/挑戰(zhàn) | 主要應(yīng)用 | 參考 |
|---|---|---|---|---|---|---|
| 胰腺祖細(xì)胞 | 胰腺發(fā)育過程中的前腸內(nèi)胚層 | 胰腺內(nèi)分泌細(xì)胞(β、α、δ、PP)和外分泌細(xì)胞(腺泡、導(dǎo)管)。 | 與糖尿病治療直接相關(guān)的是產(chǎn)生胰島素的β細(xì)胞 | 難以分離和擴(kuò)增;譜系限制了其更廣泛的應(yīng)用。 | 糖尿病治療;胰腺再生;疾病建模 | [ 19 , 23 ] |
| 胚胎干細(xì)胞(ESCs) | 囊胚內(nèi)細(xì)胞團(tuán)(受精后4-5天) | 除胎盤外,可形成所有身體組織。 | 多能性的黃金標(biāo)準(zhǔn);強(qiáng)大的分化能力 | 倫理考量;免疫排斥風(fēng)險(xiǎn) | 發(fā)育生物學(xué);再生醫(yī)學(xué);細(xì)胞治療研究 | [ 19 , 33 ] |
| 誘導(dǎo)多能干細(xì)胞(iPSCs) | 重編程的成體體細(xì)胞(成纖維細(xì)胞;Oct4、Sox2、Klf4、c-Myc) | 可以分化成幾乎所有體細(xì)胞類型 | 避免了胚胎干細(xì)胞的倫理問題;針對(duì)特定患者;無限擴(kuò)增 | 誘導(dǎo)效率低;存在遺傳不穩(wěn)定和腫瘤發(fā)生的風(fēng)險(xiǎn) | 疾病建模;藥物篩選;再生醫(yī)學(xué) | [ 34 , 35 ] |
| 間充質(zhì)干細(xì)胞(MSCs) | 成人組織(骨髓、脂肪組織、臍帶等) | 中胚層譜系:成骨細(xì)胞、軟骨細(xì)胞、脂肪細(xì)胞 | 易于分離;具有強(qiáng)大的免疫調(diào)節(jié)和抗炎特性;腫瘤風(fēng)險(xiǎn)低。 | 分化譜有限;供體間存在差異 | 骨科修復(fù);心血管治療;免疫調(diào)節(jié);組織工程 | [ [36] , [37] , [38] ] |
| 基因編輯細(xì)胞(低免疫原性PEC/β細(xì)胞) | 利用 hESCs/iPSCs 衍生的內(nèi)分泌譜系進(jìn)行基因工程改造(例如,通過 CRISPR 編輯 HLA) | β樣或胰腺內(nèi)胚層經(jīng)基因工程改造以逃避免疫反應(yīng) | 免疫原性降低;可采用同種異體“現(xiàn)成”策略 | 監(jiān)管審查;免疫逃逸的持久性;脫靶風(fēng)險(xiǎn) | 無需全身免疫抑制的同種異體β細(xì)胞替代療法 | [ [39] , [40] , [41] ] |
| 公司 | 成立年份/總部 | 領(lǐng)導(dǎo)項(xiàng)目 | 技術(shù)重點(diǎn) | 臨床試驗(yàn)狀態(tài) | 要點(diǎn) | 參考資料 |
|---|---|---|---|---|---|---|
ViaCyte | 1999年/美國圣地亞哥 | PEC-Encap(VC-01;NCT02265809) PEC-Direct(VC-02;NCT03163511) VCTX210A(PEC-QT;NCT05210530;采用 CRISPR 療法) | 胚胎干細(xì)胞衍生的胰腺祖細(xì)胞;封裝裝置;基因編輯的免疫逃逸細(xì)胞 | 1/2期臨床試驗(yàn)已完成(PEC-Encap、PEC-Direct);PEC-QT處于早期臨床階段(2025年)。 | 2022年被Vertex以3.2億美元收購;干細(xì)胞衍生β細(xì)胞替代療法的先驅(qū);封裝裝置面臨纖維化挑戰(zhàn) | [ 42 , 43 ] |
Vertex制藥公司 | 1989年/美國波士頓 | VX-880(NCT04786262;Zimislecel) VX-264(TrialTroveID-492,327) | 誘導(dǎo)多能干細(xì)胞衍生的胰島素分泌細(xì)胞;門靜脈輸注;封裝裝置 | VX-264 處于早期臨床階段;VX-880 正在進(jìn)行 1/2/3 期關(guān)鍵性試驗(yàn)(2024-2025 年) | 首例患者于2021年實(shí)現(xiàn)胰島素非依賴性;VX-880有望在2026年提交監(jiān)管審批。 | [ 44 , 45 ] |
Sernova公司 | 2008年/加拿大安大略省 | 細(xì)胞袋系統(tǒng)(Sernova 的細(xì)胞袋;NCT03513939) | 植入供體胰島或干細(xì)胞衍生β細(xì)胞的生物工程皮下囊袋 | Sernova公司用于治療性胰島移植的細(xì)胞袋的安全性和有效性的1/2期研究;中期數(shù)據(jù)顯示C肽生成和HbA1c<7.0%。 | 2025年更名為Sernova Biotherapeutics Inc.;已證實(shí)可促進(jìn)血管生成并維持胰島細(xì)胞的長期存活;正在拓展平臺(tái),開發(fā)干細(xì)胞衍生療法。 | [ 46 , 47 ] |
諾和諾德 | 1989年 / 丹麥巴格斯韋德 | 口服索馬魯肽治療 2 型糖尿病患者的心血管安全性研究 (NCT02692716); 新藥 NNC0363-1063 治療 1 型糖尿病患者的研究( NCT06685185 ) | 干細(xì)胞衍生的β細(xì)胞可用于治療1型糖尿病和2型糖尿病 | 已于2025年10月停止細(xì)胞療法研發(fā)工作。 | 已于2025年10月停止細(xì)胞療法研發(fā)工作。 | [ 48 , 49 ] |
在此基礎(chǔ)上,以ViaCyte、Vertex等為代表的眾多機(jī)構(gòu)積極投身于干細(xì)胞衍生胰腺祖細(xì)胞、封裝裝置以及基因編輯免疫逃逸細(xì)胞系的臨床探索(表2)。2000年至2025年間,相關(guān)臨床試驗(yàn)數(shù)量已超過150項(xiàng),標(biāo)志著該領(lǐng)域的研究熱情與快速發(fā)展,旨在克服傳統(tǒng)移植療法的瓶頸。
四、挑戰(zhàn)與未來方向
盡管進(jìn)展令人鼓舞,干細(xì)胞療法邁向常規(guī)臨床仍面臨嚴(yán)峻挑戰(zhàn):免疫排斥反應(yīng)、移植細(xì)胞長期存活與功能維持、致瘤風(fēng)險(xiǎn)及大規(guī)模生產(chǎn)制造等均亟待攻克。封裝技術(shù)雖旨在保護(hù)移植物,但異物反應(yīng)與血管化不足限制了其長期療效。科學(xué)家正積極探索基因編輯、生物工程等前沿手段,終極目標(biāo)是在無需長期全身免疫抑制的條件下,實(shí)現(xiàn)患者的功能性治愈。
本文全面概述了2000年以來糖尿病干細(xì)胞療法的主要臨床試驗(yàn)。通過綜合分析試驗(yàn)設(shè)計(jì)、結(jié)果與局限性,旨在突出進(jìn)展、剖析挑戰(zhàn),并將當(dāng)前研究置于再生醫(yī)學(xué)更廣闊的發(fā)展軌跡中,著重探討干細(xì)胞療法在未來數(shù)十年如何從實(shí)驗(yàn)性前景走向常規(guī)臨床應(yīng)用。
開發(fā)干細(xì)胞衍生糖尿病療法的關(guān)鍵要素
開發(fā)干細(xì)胞衍生糖尿病療法的關(guān)鍵要素,首先在于深刻理解其多靶點(diǎn)的治療機(jī)制,并以此為基礎(chǔ)設(shè)計(jì)臨床試驗(yàn)。該療法并非僅通過單一途徑發(fā)揮作用,而是通過三種相互關(guān)聯(lián)的機(jī)制靶向糖尿病復(fù)雜的病理:直接分化為產(chǎn)生胰島素的β細(xì)胞以替代缺失的細(xì)胞、通過旁分泌信號(hào)促進(jìn)內(nèi)源性胰島再生,以及調(diào)節(jié)免疫系統(tǒng)以對(duì)抗自身免疫或炎癥損傷。
臨床前研究已在多種干細(xì)胞類型中證實(shí)了這些能力,但只有經(jīng)過嚴(yán)格設(shè)計(jì)的臨床試驗(yàn),才能將這些實(shí)驗(yàn)室發(fā)現(xiàn)轉(zhuǎn)化為確切的人體治療價(jià)值,驗(yàn)證其在實(shí)際生理環(huán)境中的安全性和有效性(圖2)。
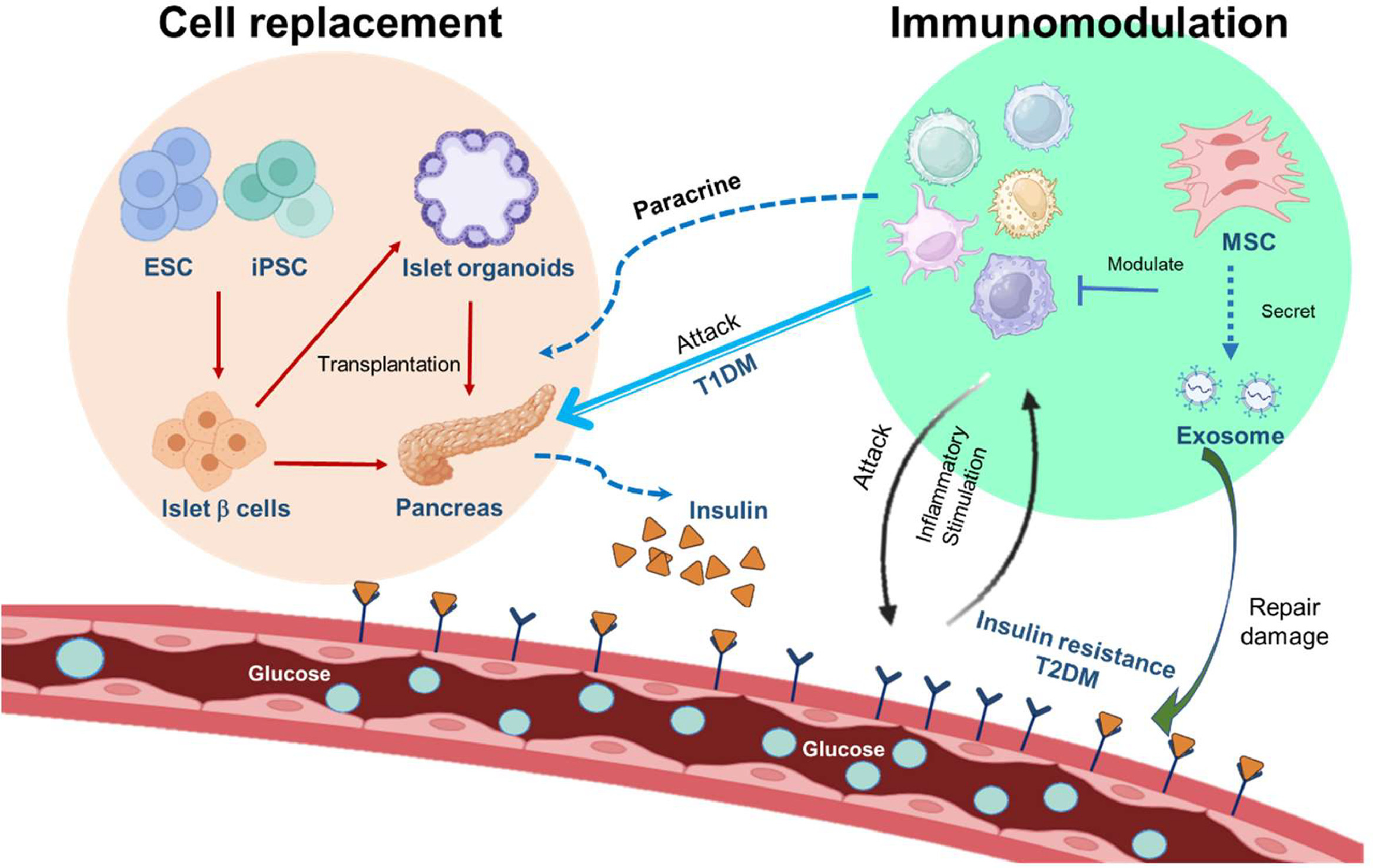
其次,借鑒并超越傳統(tǒng)的細(xì)胞替代療法經(jīng)驗(yàn)是推動(dòng)發(fā)展的關(guān)鍵。供體胰島移植(如埃德蒙頓方案)的成功,證明了細(xì)胞療法可實(shí)現(xiàn)胰島素非依賴性并獲得監(jiān)管批準(zhǔn),但其應(yīng)用受限于供體短缺和免疫排斥。因此,基于干細(xì)胞的療法必須同時(shí)解決這兩個(gè)核心障礙。一方面,它旨在提供一種可再生的細(xì)胞來源,替代稀缺的供體胰島;另一方面,早期臨床試驗(yàn)顯示干細(xì)胞可通過免疫調(diào)節(jié)發(fā)揮輔助治療作用,改善血糖控制,這提示了一種雙重策略:既通過分化細(xì)胞直接替代,又通過未分化細(xì)胞或其旁分泌作用調(diào)節(jié)病理環(huán)境,從而為1型或2型糖尿病提供更全面的治療路徑。
最后,臨床試驗(yàn)的價(jià)值遠(yuǎn)不止于驗(yàn)證療效,更是推動(dòng)療法從實(shí)驗(yàn)室走向臨床成熟的迭代平臺(tái)。試驗(yàn)不僅需建立標(biāo)準(zhǔn)化的療效終點(diǎn)(如糖化血紅蛋白降低、胰島素非依賴性),更要積累長期安全性數(shù)據(jù)、監(jiān)測遠(yuǎn)期風(fēng)險(xiǎn)。這些結(jié)果為監(jiān)管路徑建立、生產(chǎn)標(biāo)準(zhǔn)統(tǒng)一及倫理框架協(xié)調(diào)提供關(guān)鍵信息。更重要的是,每一項(xiàng)臨床試驗(yàn)均基于前人經(jīng)驗(yàn)教訓(xùn),不斷優(yōu)化細(xì)胞制備工藝、移植方案及患者篩選標(biāo)準(zhǔn)。這種迭代進(jìn)步是將干細(xì)胞療法塑造為安全、有效且可控的臨床手段,最終實(shí)現(xiàn)恢復(fù)葡萄糖穩(wěn)態(tài)與修復(fù)胰腺功能根本目標(biāo)的必由之路。
胚胎干細(xì)胞衍生療法治療糖尿病:從概念驗(yàn)證到基因編輯
胚胎干細(xì)胞(ESCs)因其多能性與無限自我更新能力,長期被視為再生醫(yī)學(xué)的基石。在糖尿病領(lǐng)域,ESCs有望生成功能性胰島β細(xì)胞,恢復(fù)內(nèi)源性胰島素分泌。21世紀(jì)初的開創(chuàng)性研究表明,ESCs可定向分化為胰腺譜系細(xì)胞,在體外產(chǎn)生表達(dá)胰島素的細(xì)胞,證實(shí)其可作為β細(xì)胞的可再生來源,有望克服尸源胰島移植的局限。
過去二十年,分化方案取得顯著進(jìn)展。早期方法獲得的β樣細(xì)胞不成熟、葡萄糖反應(yīng)性有限;逐步優(yōu)化的分化方案模擬了胚胎胰腺發(fā)育過程,產(chǎn)生了功能性更強(qiáng)的細(xì)胞(表3)。2006年,D’Amour等人開發(fā)的五步方案將人ESCs轉(zhuǎn)化為功能性胰島素分泌細(xì)胞,這些細(xì)胞能產(chǎn)生多種胰腺激素,其來源的胰腺祖細(xì)胞在移植后表現(xiàn)出體內(nèi)成熟能力,可在葡萄糖刺激下分泌胰島素并逆轉(zhuǎn)動(dòng)物模型的高血糖。
美國ViaCyte公司引領(lǐng)了ESC衍生療法的臨床轉(zhuǎn)化,是首家將人ESC來源胰腺祖細(xì)胞(PP)推進(jìn)臨床試驗(yàn)的機(jī)構(gòu)。其首款產(chǎn)品PEC-Encap(VC-01)將ESC來源胰腺祖細(xì)胞封裝于裝置內(nèi),旨在保護(hù)細(xì)胞免受免疫攻擊,同時(shí)允許營養(yǎng)物質(zhì)交換。植入后,祖細(xì)胞能成熟為胰島素生成細(xì)胞。初步I/II期試驗(yàn)證實(shí)了安全性與細(xì)胞存活率,但裝置周圍纖維化限制了長期療效。
為解決此問題,ViaCyte推出PEC-Direct(VC-02),直接植入祖細(xì)胞但需全身免疫抑制。早期試驗(yàn)顯示,1型糖尿病患者體內(nèi)可檢出C肽,證明細(xì)胞已分化為胰島素分泌細(xì)胞。最近,ViaCyte與CRISPR Therapeutics合作開發(fā)PEC-QT(VCTX210、VCTX211),利用基因編輯技術(shù)使ESC來源祖細(xì)胞逃避免疫排斥,旨在實(shí)現(xiàn)持久胰島素非依賴性且無需終身免疫抑制,標(biāo)志著該領(lǐng)域的重大進(jìn)展(表3)。
| 試驗(yàn)名稱 | 開始年份 | 贊助 | 試驗(yàn)?zāi)繕?biāo) | 試驗(yàn)/參與者編號(hào) | 細(xì)胞類型 | 主要成果 | 影響 | 參考資料 |
|---|---|---|---|---|---|---|---|---|
| 胚胎干細(xì)胞衍生療法治療糖尿病 | ||||||||
| VC-01(PEC封裝) | 2014–2019 | ViaCyte | 包埋胰腺祖細(xì)胞的安全性和存活率 | 1型糖尿病(2)/約19 | ESCs衍生的胰腺內(nèi)胚層細(xì)胞(PEC-01) | 證實(shí)細(xì)胞存活并部分成熟;檢測到C肽;纖維化限制了療效 | 封裝概念驗(yàn)證;突出異物反應(yīng)挑戰(zhàn) | [ 24 , 57 ] |
| VC-02(PEC-Direct) | 2017–2022 | ViaCyte | 評(píng)估開放式裝置中的血管化和胰島素生成情況 | 1型糖尿病(1)/約15-20 | 胚胎干細(xì)胞衍生的胰腺祖細(xì)胞 | 血管生成改善;觀察到胰島素分泌;需要全身免疫抑制治療 | 已證實(shí)胰島素功能正常;但需權(quán)衡免疫抑制負(fù)擔(dān)。 | [ 58 , 59 ] |
| VCTX210A(免疫逃逸型PEC產(chǎn)品) | 2022–2024 | ViaCyte + CRISPR Therapeutics | 評(píng)估基因編輯的低免疫原性PEC細(xì)胞的安全性和移植效果 | T1DM(1)/ ~12 | ESCs衍生的胰腺內(nèi)胚層細(xì)胞(PEC210A) | CRISPR基因編輯技術(shù)改造的免疫逃逸細(xì)胞首次人體試驗(yàn);安全性可接受;療效待定 | 基因編輯干細(xì)胞療法里程碑式試驗(yàn);有望消除免疫抑制 | [ 39 ] |
| VCTX211(下一代免疫逃逸型PEC) | 2023年至今 | ViaCyte + CRISPR Therapeutics | 工程化光電化學(xué)細(xì)胞的安全性、耐受性和有效性 | T1DM(1/2)/ ~30 | 胚胎干細(xì)胞來源的胰腺內(nèi)胚層細(xì)胞 | 正在進(jìn)行中;旨在提高耐久性和免疫逃避能力 | 有望建立可擴(kuò)展的免疫保護(hù)干細(xì)胞療法 | [ 40 ] |
| iPSCs β樣療法治療糖尿病 | ||||||||
| VX-880(全身移植) | 2021年至今 | Vertex制藥公司 | 恢復(fù)內(nèi)源性胰島素分泌;減少/停止胰島素注射 | 1 型糖尿病 ( 1 ) 伴低血糖感知障礙 / ~52 | iPSCs β樣細(xì)胞或胰腺祖細(xì)胞 | 早期患者C肽水平恢復(fù)正常,胰島素注射減少或停止;糖化血紅蛋白<7.0%;安全性良好 | 干細(xì)胞衍生胰島在人體中的概念驗(yàn)證;顯示出療效,但需要終身免疫抑制 | [ 26 , 60 ] |
| VX-264(封裝式頂點(diǎn)療法) | 2013–2025 | Vertex制藥公司 | 采用封裝策略以避免全身免疫抑制 | 1型糖尿病(1/2)/ NA | iPSCs β樣細(xì)胞或胰腺祖細(xì)胞 | 早期試點(diǎn)工作已完成;目前正在進(jìn)行以安全性和可行性為終點(diǎn)的試驗(yàn)。 | 如果成功,可減輕免疫抑制負(fù)擔(dān);解決封裝難題。 | [ 30 , 61 , 62 ] |
誘導(dǎo)多能干細(xì)胞療法治療糖尿病:從患者特異到通用型
誘導(dǎo)多能干細(xì)胞(iPSCs)的誕生為糖尿病細(xì)胞療法開辟了新路徑。通過導(dǎo)入特定轉(zhuǎn)錄因子將成體細(xì)胞重編程為多能狀態(tài),既保留了與ESC相當(dāng)?shù)姆只瘽撃埽忠?guī)避了胚胎組織的倫理爭議。這一突破使構(gòu)建患者特異性干細(xì)胞系成為可能,為自體移植減少免疫排斥奠定了基礎(chǔ)。研究者已成功將iPSCs定向誘導(dǎo)分化為胰腺譜系,獲得能響應(yīng)葡萄糖刺激并分泌胰島素的成熟β樣細(xì)胞。
臨床轉(zhuǎn)化層面,Vertex Pharmaceuticals進(jìn)展最具代表性。其核心產(chǎn)品VX-880通過門靜脈輸注移植iPSC衍生胰島素分泌細(xì)胞,2021年首例患者實(shí)現(xiàn)里程碑式的胰島素非依賴性。后續(xù)I/II期數(shù)據(jù)顯示,患者單次移植后恢復(fù)內(nèi)源性胰島素分泌,C肽持續(xù)檢出,血糖控制顯著改善,外源性胰島素依賴大幅降低。但該方案仍需配合全身免疫抑制。為此Vertex推出VX-264,采用封裝裝置保護(hù)移植細(xì)胞,旨在消除終身免疫抑制的必要性,形成直接輸注與裝置封裝并行的雙重策略。
除國際領(lǐng)軍企業(yè)外,中國學(xué)術(shù)團(tuán)隊(duì)亦取得突破。2024年,國內(nèi)合作團(tuán)隊(duì)發(fā)表首例化學(xué)誘導(dǎo)多能干細(xì)胞(CiPSCs)來源胰島移植臨床報(bào)告:將自體CiPSCs分化為胰島細(xì)胞,移植入1型糖尿病患者體內(nèi),成功實(shí)現(xiàn)功能性胰島素非依賴。這一成果驗(yàn)證了化學(xué)重編程路線的可行性,為減少供體依賴、降低免疫抑制需求提供了新的臨床證據(jù)。
盡管iPSCs衍生療法前景廣闊,仍面臨多重挑戰(zhàn):大規(guī)模生產(chǎn)符合GMP標(biāo)準(zhǔn)的iPSC衍生β細(xì)胞需嚴(yán)格質(zhì)控體系以消除致瘤風(fēng)險(xiǎn);移植細(xì)胞長期存活與功能維持有賴于生物材料、血管化策略及免疫調(diào)節(jié)技術(shù)的持續(xù)優(yōu)化。盡管如此,iPSCs技術(shù)因其個(gè)性化、符合倫理及潛在規(guī)模化應(yīng)用前景,仍被視為實(shí)現(xiàn)全球可推廣糖尿病治療的重要路徑。
間充質(zhì)干細(xì)胞療法:從細(xì)胞治療到無細(xì)胞制劑
間充質(zhì)干細(xì)胞(MSCs)是糖尿病領(lǐng)域研究最為廣泛的干細(xì)胞類型之一。其優(yōu)勢在于易于獲取、免疫原性低及強(qiáng)大的免疫調(diào)節(jié)與旁分泌作用。與ESC或iPSC不同,MSCs是來源于骨髓、脂肪、臍帶或牙髓的成體祖細(xì)胞,其治療應(yīng)用并非主要基于直接分化為胰島素分泌細(xì)胞,而是通過調(diào)節(jié)免疫微環(huán)境、改善代謝發(fā)揮效用。
臨床試驗(yàn)已證實(shí)MSCs可改善1型及2型糖尿病患者的代謝指標(biāo)。Hu等報(bào)道,1型糖尿病患者靜脈輸注異體MSCs可提高C肽水平、降低胰島素需求。Xu等通過薈萃分析證實(shí),MSCs療法安全有效,可適度改善血糖控制。Zang等報(bào)道,MSCs治療顯著改善1型糖尿病患者C肽水平并降低胰島素需求。進(jìn)一步研究表明,臍帶來源MSCs可增強(qiáng)2型糖尿病患者血糖控制、降低HbA1c。
近年來,該領(lǐng)域正經(jīng)歷從“細(xì)胞治療”向“無細(xì)胞治療”的范式演進(jìn)。MSC來源外泌體作為新型治療劑,能遞送調(diào)節(jié)免疫與代謝通路的生物活性分子,規(guī)避全細(xì)胞療法的致瘤風(fēng)險(xiǎn),提高產(chǎn)品可重復(fù)性與規(guī)模化生產(chǎn)潛力。早期臨床探索如Exo-HWS試驗(yàn)正驗(yàn)證這一方向可行性。然而,MSCs療法仍面臨諸多挑戰(zhàn):直接替代β細(xì)胞能力有限、產(chǎn)品異質(zhì)性大、治療效果可能短暫需重復(fù)給藥、臨床應(yīng)用標(biāo)準(zhǔn)化面臨監(jiān)管障礙。
展望未來,MSCs療法的價(jià)值將更多體現(xiàn)在聯(lián)合治療策略中。其免疫調(diào)節(jié)與代謝支持功能有望與ESC/iPSC來源β細(xì)胞替代療法形成協(xié)同,在實(shí)現(xiàn)胰島素分泌重建的同時(shí),為移植細(xì)胞提供免疫保護(hù)微環(huán)境。推動(dòng)MSC來源外泌體等無細(xì)胞制劑的標(biāo)準(zhǔn)化與規(guī)模化生產(chǎn),開展大規(guī)模隨機(jī)對(duì)照試驗(yàn)驗(yàn)證其長期療效與安全性,將是該領(lǐng)域走向臨床成熟的關(guān)鍵路徑。MSCs雖難以獨(dú)立實(shí)現(xiàn)治愈,但注定將成為糖尿病綜合干細(xì)胞治療策略中不可或缺的組成部分。
用于干細(xì)胞治療糖尿病的封裝技術(shù)
封裝技術(shù):從物理屏障到免疫逃逸
封裝技術(shù)在干細(xì)胞衍生糖尿病療法中扮演著免疫保護(hù)的核心角色。它通過生物材料構(gòu)建物理屏障,將移植細(xì)胞與宿主免疫系統(tǒng)隔離,從而避免或減少對(duì)全身免疫抑制的依賴。這種屏障在保護(hù)細(xì)胞的同時(shí),允許氧氣、營養(yǎng)物質(zhì)、葡萄糖及胰島素等小分子自由雙向擴(kuò)散,確保細(xì)胞能感知血糖變化并響應(yīng)性分泌胰島素。該技術(shù)旨在破解供體稀缺與終身免疫抑制兩大瓶頸,目前主要形成宏觀封裝(可回收裝置)與微觀封裝(水凝膠包裹)兩大策略。
臨床應(yīng)用中,封裝技術(shù)經(jīng)歷了顯著迭代(圖3)。最具代表性的ViaCyte公司PEC-Encap(VC-01)率先將ESC來源胰腺祖細(xì)胞封裝植入人體,早期試驗(yàn)證實(shí)安全性,但裝置誘發(fā)的異物反應(yīng)導(dǎo)致纖維化與血管化不足,限制了細(xì)胞存活。為規(guī)避此問題,ViaCyte一方面推出需配合免疫抑制的PEC-Direct(VC-02),另一方面與CRISPR Therapeutics合作開發(fā)PEC-QT,通過基因編輯賦予細(xì)胞免疫逃逸能力。其他創(chuàng)新平臺(tái)如Sernova的Cell Pouch System側(cè)重于在植入前構(gòu)建血管化組織微環(huán)境;Beta-O2 Technologies的βAir裝置則通過集成氧氣室維持細(xì)胞活力。
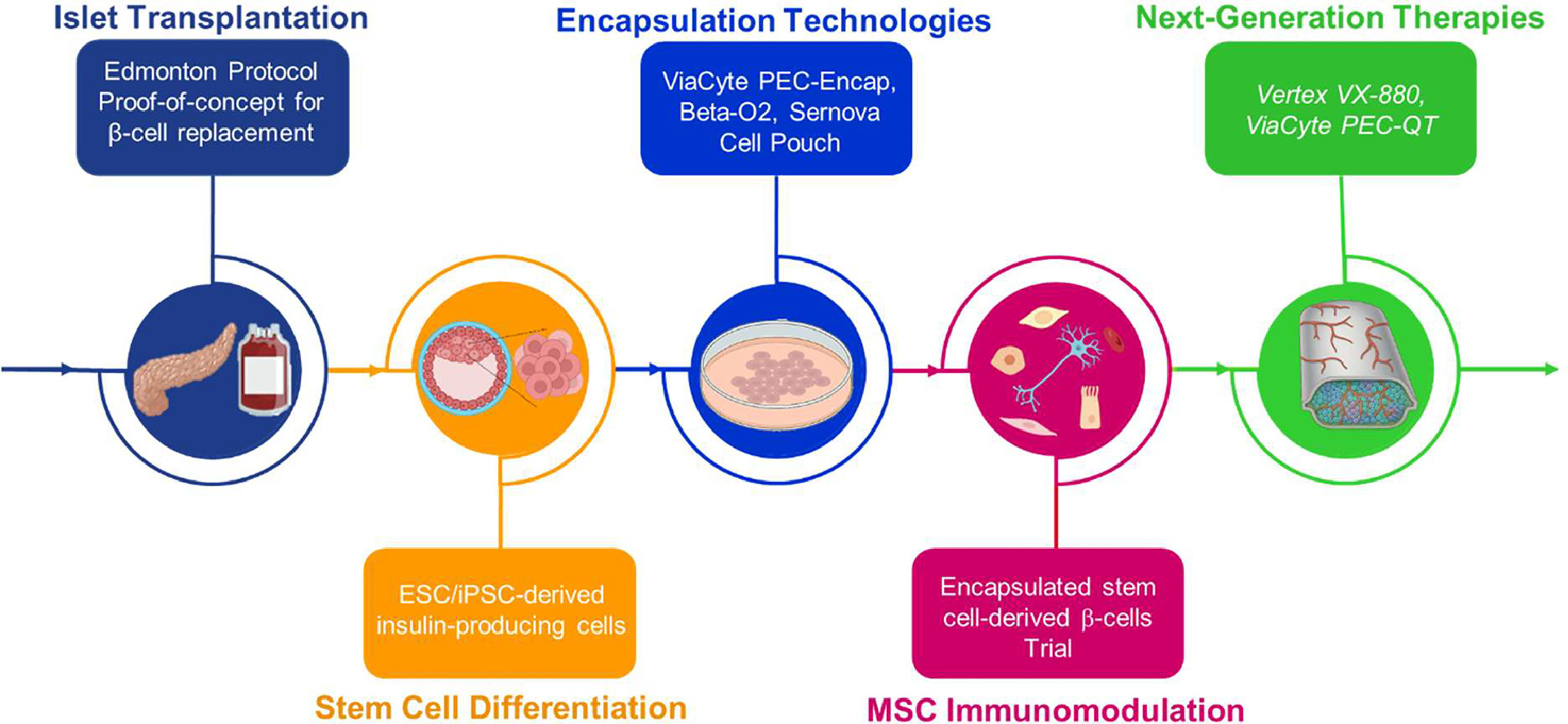
從技術(shù)演進(jìn)看,封裝技術(shù)正從單純的物理屏障向生物工程與基因編輯相融合的復(fù)合型平臺(tái)發(fā)展。早期技術(shù)聚焦于用半透膜保護(hù)供體胰島;隨后研究重點(diǎn)轉(zhuǎn)向開發(fā)生物相容性更好、能有效減少纖維化并促進(jìn)血管化的新材料;最新突破方向是將基因編輯技術(shù)引入,構(gòu)建具有免疫逃逸能力的干細(xì)胞衍生β細(xì)胞,實(shí)現(xiàn)再生醫(yī)學(xué)與生物工程的深度融合。這一演進(jìn)路徑的終極目標(biāo),是在無需全身免疫抑制條件下,利用可再生干細(xì)胞來源實(shí)現(xiàn)規(guī)模化、持久且安全的胰島素非依賴性治療。
未來干細(xì)胞治療糖尿病的挑戰(zhàn)都有哪些?
首先,在科學(xué)與技術(shù)層面,免疫排斥和安全性是根本性障礙。即使使用自體誘導(dǎo)多能干細(xì)胞(iPSC)衍生的β細(xì)胞,在1型糖尿病自身免疫背景下,移植細(xì)胞仍可能被機(jī)體原有的免疫記憶攻擊。致瘤性風(fēng)險(xiǎn)同樣嚴(yán)峻,若多能干細(xì)胞分化不完全,殘留的未分化細(xì)胞可能導(dǎo)致畸胎瘤形成,因此需要開發(fā)極致的純化和安全檢測技術(shù)。此外,如何確保大規(guī)模生產(chǎn)的每一批次β細(xì)胞都具有成熟的功能性和葡萄糖反應(yīng)性,以及如何解決移植后細(xì)胞因纖維化包裹、氧合不足和血管化不良而導(dǎo)致的長期存活率低下,都是亟待突破的技術(shù)瓶頸。
| 挑戰(zhàn) | 影響 | 潛在解決方案 | 參考 |
|---|---|---|---|
| 免疫排斥 | 移植細(xì)胞丟失;需要免疫抑制治療 | 基因編輯(CRISPR/Cas9);封裝裝置;免疫療法;通用供體細(xì)胞系 | [ 22 , 24 ] |
| 致瘤性 | 安全風(fēng)險(xiǎn)(畸胎瘤形成、遺傳不穩(wěn)定性) | 純化;嚴(yán)格的質(zhì)量控制;自殺基因(誘導(dǎo)型caspase-9);基因組穩(wěn)定性檢測 | [ 98 , 99 ] |
| 分化變異性 | 胰島素分泌不穩(wěn)定;細(xì)胞群體異質(zhì)性 | 標(biāo)準(zhǔn)化方案;生物反應(yīng)器優(yōu)化;類器官系統(tǒng);階段特異性生長因子 | [ 35 , 100 ] |
| 長期生存 | 由于缺氧、纖維化和炎癥導(dǎo)致移植腎功能下降 | 先進(jìn)生物材料;血管化策略;與間充質(zhì)干細(xì)胞共移植;抗纖維化支架 | [ 24 , 99 ] |
| 生產(chǎn)規(guī)模 | 全球準(zhǔn)入受限且成本高昂 | 可擴(kuò)展的生物工藝;自動(dòng)化;封閉式GMP生產(chǎn);國際細(xì)胞庫 | [ 98 ] |
| 監(jiān)管和倫理問題 | 臨床應(yīng)用緩慢、全球標(biāo)準(zhǔn)分散、公眾接受度低以及道德爭議 | 優(yōu)先選擇誘導(dǎo)多能干細(xì)胞來源;替代捐贈(zèng)者來源;統(tǒng)一的國際準(zhǔn)則;透明的治理框架; | [ 3 , 52 , 98 , 99 ] |
其次,在生產(chǎn)、臨床轉(zhuǎn)化與監(jiān)管層面,標(biāo)準(zhǔn)化和可及性面臨巨大挑戰(zhàn)。全球范圍內(nèi)對(duì)數(shù)以十億計(jì)功能性β細(xì)胞的需求,要求建立符合良好生產(chǎn)規(guī)范的超大規(guī)模擴(kuò)增體系。目前尚缺乏國際公認(rèn)的效力、純度和安全性評(píng)估檢測方法,導(dǎo)致不同臨床試驗(yàn)間的終點(diǎn)指標(biāo)(如糖化血紅蛋白降低與胰島素完全依賴)難以橫向比較。各地區(qū)碎片化的監(jiān)管審批框架和漫長的審查流程,進(jìn)一步延緩了療法的轉(zhuǎn)化應(yīng)用。封裝裝置雖有望解決免疫排斥,但其自身也面臨著纖維化過度、氧合不足以及長期生物相容性和耐久性等工程設(shè)計(jì)難題。
最后,在疾病特異性和倫理層面,治療策略需要精準(zhǔn)匹配病理機(jī)制。1型糖尿病必須解決自身免疫復(fù)發(fā)問題,這意味著單純的細(xì)胞替代可能需要聯(lián)合免疫調(diào)節(jié)策略;而2型糖尿病則需要應(yīng)對(duì)全身性胰島素抵抗,否則移植的β細(xì)胞可能因代謝負(fù)荷過重而失效。此外,圍繞胚胎干細(xì)胞使用的倫理爭議,包括供體組織來源、患者知情同意和公平獲取醫(yī)療資源等問題,依然是必須審慎應(yīng)對(duì)的社會(huì)議題。克服這些挑戰(zhàn),需要細(xì)胞工程、生物材料、規(guī)模化生產(chǎn)和個(gè)性化醫(yī)療策略的協(xié)同進(jìn)步。
未來干細(xì)胞治療糖尿病的方向
基于干細(xì)胞的糖尿病治療未來將深度融合基因編輯、生物材料與組織工程,致力于開發(fā)能夠逃避免疫攻擊的“通用型”細(xì)胞產(chǎn)品。以CRISPR/Cas9技術(shù)為核心的免疫逃逸干細(xì)胞是當(dāng)前最活躍的研究方向,通過敲除移植細(xì)胞的免疫識(shí)別位點(diǎn),使其在不需或僅需極少免疫抑制的情況下長期存活(圖4)。
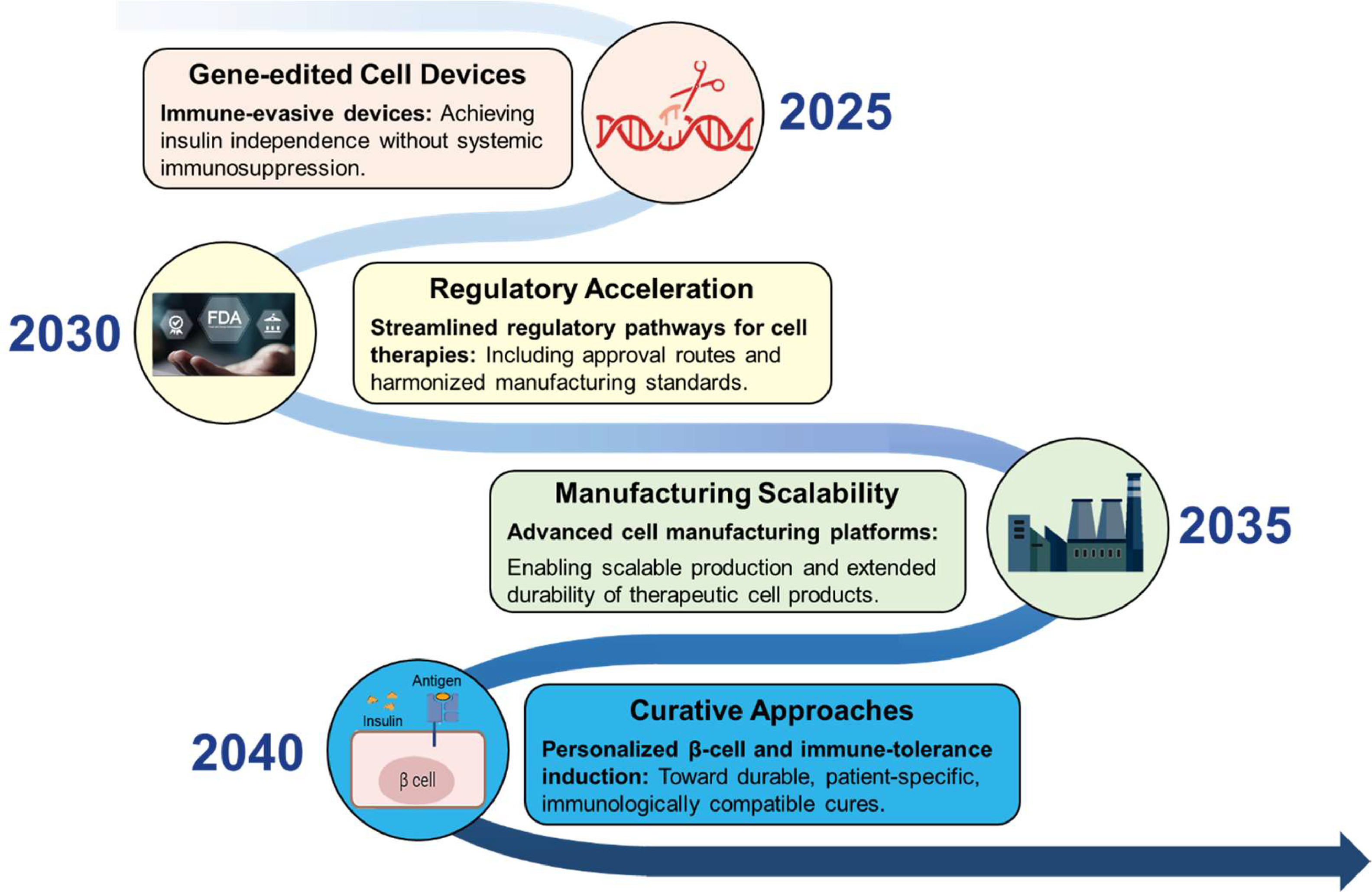
ViaCyte與CRISPR Therapeutics合作的PEC-QT項(xiàng)目以及CTX211等產(chǎn)品已進(jìn)入早期臨床試驗(yàn),旨在驗(yàn)證這一策略的可行性。與此同時(shí),封裝技術(shù)正從單純的物理屏障向智能化、功能化平臺(tái)演進(jìn),新一代裝置將整合免疫調(diào)節(jié)涂層、促血管化設(shè)計(jì)和實(shí)時(shí)生物傳感功能,以解決纖維化包裹和氧合不足等關(guān)鍵難題,最終實(shí)現(xiàn)無需免疫抑制的胰島素非依賴性。
| 未來方向 | 關(guān)鍵創(chuàng)新 | 預(yù)期影響 | 示例 | 參考資料 |
|---|---|---|---|---|
| 免疫逃逸干細(xì)胞 | 經(jīng) CRISPR 編輯的具有多基因免疫隱蔽功能的 β 細(xì)胞(例如,B2M/CIITA 敲除;HLA-E/HLA-G/PD-L1 過表達(dá));NK/T 細(xì)胞活化降低的“隱形”胰島 | 無需維持免疫抑制即可擺脫胰島素依賴;排斥反應(yīng)發(fā)生率更低;適用范圍更廣,包括兒童1型糖尿病患者。 | ViaCyte-CRISPR PEC-QT (VCTX210);通用低免疫原性iPSCs細(xì)胞系;HLA工程學(xué)術(shù)聯(lián)盟 | [ 111 , 112 ] |
| 封裝 | 抗纖維化、兩性離子和聚乙二醇化生物材料;巨噬細(xì)胞重編程涂層;氧合/血管生成裝置設(shè)計(jì);具有優(yōu)化傳質(zhì)的微/宏囊化 | 長期移植存活率高,異物反應(yīng)降低;血糖控制穩(wěn)定;可回收性好且安全 | ViaCyte PEC-Encap;Sernova細(xì)胞囊;藻酸鹽變體(三唑/氟化藻酸鹽);產(chǎn)氧支架 | [ 113 , 114 ] |
| 制造業(yè) | 符合GMP標(biāo)準(zhǔn)的封閉式工作流程;具備在線監(jiān)測功能的自動(dòng)化區(qū)分;可擴(kuò)展的攪拌罐/灌注式生物反應(yīng)器;穩(wěn)健的釋放和效力檢測 | 可擴(kuò)展的全球療法,批次可重復(fù);更低的藥品成本;更快的批次放行速度和供應(yīng)可靠性 | 立式輪式攪拌罐生物反應(yīng)器;標(biāo)準(zhǔn)化的β細(xì)胞分化標(biāo)準(zhǔn)操作規(guī)程;質(zhì)量控制指標(biāo)(C肽分泌、葡萄糖反應(yīng)性、無菌性、核型) | [ [115] , [116] , [117] ] |
| 聯(lián)合療法 | 間充質(zhì)干細(xì)胞共移植用于免疫調(diào)節(jié);Treg細(xì)胞誘導(dǎo);抗原特異性耐受(例如,耐受性樹突狀細(xì)胞);β細(xì)胞替代加免疫重置(例如,低劑量生物制劑) | 療效增強(qiáng),自身免疫反應(yīng)和移植失敗率降低;移植成功率和血管化改善;低血糖事件減少 | 間充質(zhì)干細(xì)胞+胰島替代療法試點(diǎn)研究;基于調(diào)節(jié)性T細(xì)胞的耐受性試驗(yàn);輔助低劑量抗CD3/IL-2療法 | [ 29 , 38 , 118 ] |
| 生物工程 | 血管化胰島構(gòu)建體的3D生物打印;芯片類器官微流控技術(shù);用于快速灌注的內(nèi)皮細(xì)胞和周細(xì)胞共培養(yǎng);智能生物傳感器集成 | 構(gòu)建具有生理胰島素動(dòng)力學(xué)、更佳耐久性和實(shí)時(shí)監(jiān)測功能的生物工程胰腺 | 生物打印胰島支架;芯片胰島平臺(tái);具有內(nèi)皮網(wǎng)絡(luò)的血管化類器官 | [ 119 , 120 ] |
| 臨床擴(kuò)展 | 采用標(biāo)準(zhǔn)化終點(diǎn)指標(biāo)(C肽曲線下面積、血糖達(dá)標(biāo)時(shí)間、嚴(yán)重低血糖發(fā)生率、外源性胰島素減少量)的II/III期多中心試驗(yàn);長期安全性注冊(cè)研究 | 監(jiān)管部門批準(zhǔn)和全球推廣;支付方覆蓋范圍;來自不同人群的證據(jù) | Vertex VX-880/VX-264 試驗(yàn);ViaCyte 項(xiàng)目;持久療效的協(xié)調(diào)注冊(cè)研究 | [ 61 ] |
| 政策框架 | 細(xì)胞療法的國際統(tǒng)一監(jiān)管;加速審批途徑(RMAT、PRIME、Sakigake);上市后承諾;符合倫理的采購和公平獲取模式 | 更快、更安全的翻譯;全球標(biāo)準(zhǔn)化;公平分配和價(jià)格合理 | FDA RMAT、EMA PRIME、PMDA Sakigake;WHO/ISCT 指南;基于價(jià)值的報(bào)銷試點(diǎn)項(xiàng)目 | [ 121 ] |
在生產(chǎn)與制造層面,實(shí)現(xiàn)大規(guī)模、可重復(fù)且標(biāo)準(zhǔn)化的細(xì)胞生產(chǎn)是未來十年臨床轉(zhuǎn)化的核心任務(wù)。隨著誘導(dǎo)多能干細(xì)胞(iPSC)技術(shù)的成熟,治療模式將呈現(xiàn)患者特異性與通用型供體細(xì)胞并存的格局。生物反應(yīng)器系統(tǒng)的開發(fā)旨在穩(wěn)定生成數(shù)十億級(jí)的功能性胰島β細(xì)胞,以滿足全球日益增長的患者需求。同時(shí),國際社會(huì)亟需統(tǒng)一分化方案、效力檢測與安全性評(píng)估標(biāo)準(zhǔn),確保不同地區(qū)、不同中心生產(chǎn)的細(xì)胞產(chǎn)品具有一致的質(zhì)量和療效。3D生物打印與胰腺類器官技術(shù)的進(jìn)步,將進(jìn)一步推動(dòng)構(gòu)建具有復(fù)雜血管結(jié)構(gòu)和微環(huán)境的可移植組織,為實(shí)現(xiàn)完全生物工程化胰腺替代奠定基礎(chǔ)。
面對(duì)糖尿病復(fù)雜的病理機(jī)制,聯(lián)合治療策略將成為提升療效的關(guān)鍵方向。將間充質(zhì)干細(xì)胞(MSC)與ESC/iPSC衍生的β細(xì)胞聯(lián)合應(yīng)用,可同時(shí)發(fā)揮免疫調(diào)節(jié)、旁分泌支持與胰島素分泌的協(xié)同作用。此外,干細(xì)胞移植與免疫療法(如檢查點(diǎn)抑制劑、耐受性疫苗)的組合,有望預(yù)防1型糖尿病患者自身免疫病的復(fù)發(fā)。針對(duì)2型糖尿病,干細(xì)胞治療則需與生活方式干預(yù)或代謝藥物相結(jié)合,以克服胰島素抵抗對(duì)移植細(xì)胞功能的影響。這些多維度的聯(lián)合策略體現(xiàn)了從單純細(xì)胞替代向系統(tǒng)功能重建的理念轉(zhuǎn)變。
最終,干細(xì)胞治療糖尿病的未來發(fā)展高度依賴于政策創(chuàng)新、倫理框架完善與全球化協(xié)作。開展大規(guī)模多中心3期臨床試驗(yàn),驗(yàn)證療法的長期安全性、有效性及持久性,并建立包括胰島素非依賴性、糖化血紅蛋白降低和低血糖預(yù)防在內(nèi)的標(biāo)準(zhǔn)化終點(diǎn)指標(biāo),是獲得監(jiān)管批準(zhǔn)的必要條件。同時(shí),政策制定者需推動(dòng)監(jiān)管框架的國際協(xié)調(diào),解決胚胎干細(xì)胞使用、供者知情同意、治療公平可及等倫理議題。
展望未來,根據(jù)文本提供的路線圖,該領(lǐng)域正沿著“2025年免疫保護(hù)創(chuàng)新→2030年可擴(kuò)展生產(chǎn)→2035年監(jiān)管優(yōu)化→2040年治愈性療法”的軌跡演進(jìn),最終通過再生醫(yī)學(xué)、生物工程與政策創(chuàng)新的融合,實(shí)現(xiàn)持久胰島素非依賴性和全球可及的變革性目標(biāo)。
結(jié)論
臨床證據(jù)已明確證實(shí)干細(xì)胞療法的潛力與局限。一方面,胰島移植的成功(如埃德蒙頓方案)及Vertex公司VX-880項(xiàng)目實(shí)現(xiàn)胰島素非依賴的案例,確證了通過細(xì)胞替代恢復(fù)胰島素分泌功能的可行性。另一方面,供體極度短缺、需終身使用免疫抑制劑、移植細(xì)胞長期存活率低以及1型糖尿病中自身免疫可能復(fù)發(fā)等問題,構(gòu)成了臨床轉(zhuǎn)化的核心障礙。間充質(zhì)干細(xì)胞的臨床研究雖展示了其免疫調(diào)節(jié)與代謝支持的輔助價(jià)值,但其本身無法替代胰島素生成,凸顯了單純依靠MSCs的局限性。
要實(shí)現(xiàn)常規(guī)臨床應(yīng)用,必須克服技術(shù)、生產(chǎn)和監(jiān)管的系統(tǒng)性挑戰(zhàn)。未來的關(guān)鍵在于將基因編輯(如CRISPR技術(shù)構(gòu)建免疫逃逸細(xì)胞)、先進(jìn)封裝技術(shù)(解決免疫排斥與細(xì)胞存活)和規(guī)模化生物反應(yīng)器生產(chǎn)進(jìn)行深度融合。產(chǎn)業(yè)界正積極投入這些方向——市場預(yù)測顯示,該領(lǐng)域?qū)?024年的約52億美元增長至2033年的128億美元。然而,最終成功還取決于開展設(shè)計(jì)嚴(yán)謹(jǐn)?shù)腎II期臨床試驗(yàn)以驗(yàn)證長期療效與安全性,并建立全球統(tǒng)一的監(jiān)管標(biāo)準(zhǔn)和倫理框架,確保治療的可及性與公平性。
參考資料:[1]:https://www.sciencedirect.com/science/article/abs/pii/S1262363626000170
免責(zé)說明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信