全球首款!兩款干細(xì)胞療法獲批日本,用于心衰和帕金森病
2026年2月,誘導(dǎo)多能干細(xì)胞(iPS細(xì)胞)技術(shù)迎來了歷史性時(shí)刻。日本厚生勞動(dòng)省專家小組正式批準(zhǔn)兩款iPS細(xì)胞來源的再生醫(yī)學(xué)產(chǎn)品有條件上市,分別用于治療重癥心力衰竭和帕金森病。這是全球首次有iPS細(xì)胞治療產(chǎn)品獲得監(jiān)管放行,標(biāo)志著這項(xiàng)源于日本、曾獲諾貝爾獎(jiǎng)的技術(shù),歷經(jīng)20年探索,正式從“實(shí)驗(yàn)室故事”邁入“臨床實(shí)用階段”。

借此馬年開工之際,這兩款產(chǎn)品的獲批不僅為醫(yī)學(xué)界注入強(qiáng)心針,也象征著再生醫(yī)學(xué)領(lǐng)域“一馬當(dāng)先”的突破。
兩款劃時(shí)代產(chǎn)品:修復(fù)心臟與大腦
本次獲批的兩款產(chǎn)品均利用了iPS細(xì)胞的分化潛能,通過將健康供體的iPS細(xì)胞誘導(dǎo)分化為特定功能細(xì)胞,來修復(fù)受損的人體組織。
- ReHeart(重癥心衰治療):由大阪大學(xué)衍生企業(yè)Cuorips開發(fā)。該產(chǎn)品將iPS細(xì)胞誘導(dǎo)分化為心肌細(xì)胞,制成約0.1毫米厚的超薄心肌細(xì)胞片。通過手術(shù)貼附于受損心臟表面后,細(xì)胞片可通過分泌細(xì)胞因子促進(jìn)血管新生與心肌組織修復(fù),專門用于重癥缺血性心肌病的治療。
- Amshepri(帕金森病治療):由住友制藥基于京都大學(xué)的研究成果開發(fā)。該產(chǎn)品將iPS細(xì)胞誘導(dǎo)為多巴胺神經(jīng)前體細(xì)胞,通過立體定向手術(shù)精確移植至腦內(nèi)殼核。移植后的細(xì)胞能夠分化為功能性多巴胺能神經(jīng)元,從而補(bǔ)充帕金森病患者大腦中缺失的多巴胺,改善運(yùn)動(dòng)功能。
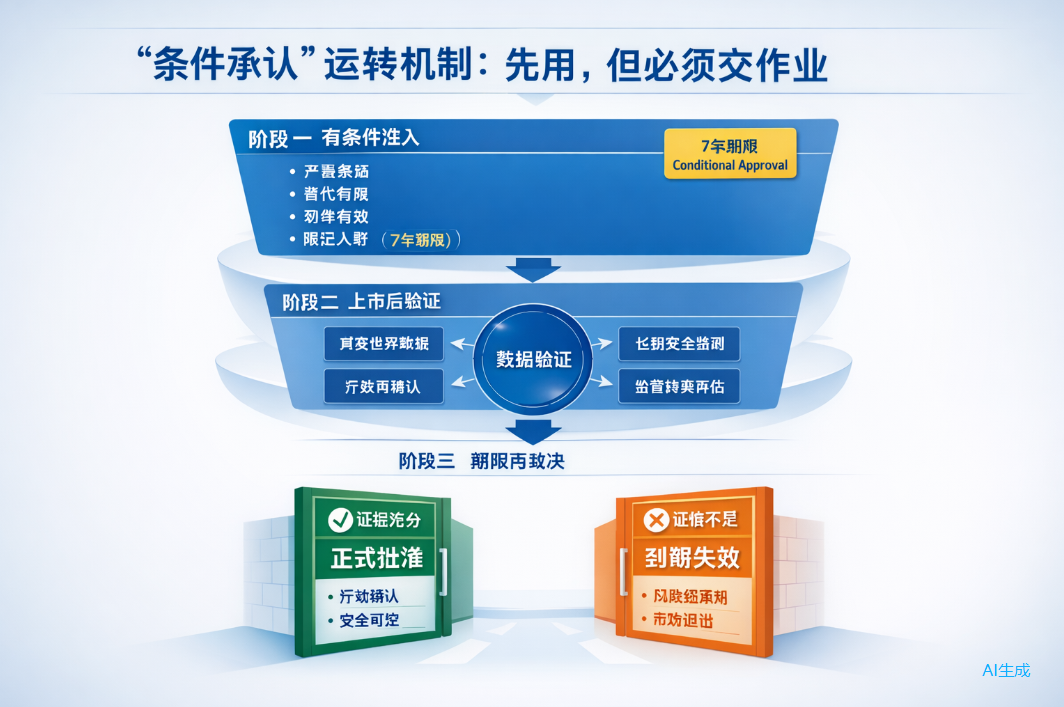
“7年條件承認(rèn)”:加速背后的嚴(yán)謹(jǐn)邏輯
這兩款產(chǎn)品并非傳統(tǒng)意義上的“完全批準(zhǔn)”,而是通過日本特有的“條件及期限付承認(rèn)”(有條件限時(shí)審批)制度獲批。

這一制度的本質(zhì)是“先讓符合條件的患者用上”,同時(shí)要求企業(yè)在最長(zhǎng)7年的“條件承認(rèn)期”內(nèi),完成更大樣本的臨床驗(yàn)證。監(jiān)管機(jī)構(gòu)明確表示,這一機(jī)制的前提是早期數(shù)據(jù)已“可預(yù)測(cè)有效且安全性已確認(rèn)”。企業(yè)必須在期限內(nèi)提交能支撐轉(zhuǎn)為完全批準(zhǔn)的證據(jù),如果有效性無法確認(rèn),批準(zhǔn)將到期失效。
因此,這一里程碑并非監(jiān)管“放水”,而是在確保安全底線的前提下,為高風(fēng)險(xiǎn)、高潛力的再生醫(yī)療產(chǎn)品開辟了一條“先上市、后補(bǔ)證”的現(xiàn)實(shí)通道。歷史上,也曾有產(chǎn)品因后續(xù)證據(jù)不足而在該機(jī)制下被撤回,這提醒著行業(yè):加速不是終點(diǎn),補(bǔ)證才是勝負(fù)手。
臨床數(shù)據(jù):初步驗(yàn)證安全性與有效性
兩款產(chǎn)品的獲批基于有限的但令人鼓舞的早期臨床數(shù)據(jù):
ReHeart:在納入8例重癥心衰患者的臨床研究中,術(shù)后3個(gè)月患者心臟功能顯著改善,所有患者癥狀得到緩解,且在觀察期內(nèi)未發(fā)現(xiàn)腫瘤形成。
Amshepri:在納入7例帕金森病患者的臨床研究中,6例療效可評(píng)估者中有4例運(yùn)動(dòng)功能獲得明確改善,部分患者甚至恢復(fù)了日常活動(dòng)能力。PET影像學(xué)證實(shí)移植細(xì)胞可在腦內(nèi)存活并分泌多巴胺,且無腫瘤形成。該研究結(jié)果已發(fā)表于國(guó)際頂尖期刊《自然》(Nature)。

展望:從科學(xué)可行到制度可行
iPS細(xì)胞由京都大學(xué)山中伸彌教授于2006年首次在實(shí)驗(yàn)室中制備成功,2012年即榮獲諾貝爾獎(jiǎng)。然而,從“能做”到“能批”,這十多年來,科學(xué)家們一直在攻克規(guī)模化制造、批間一致性以及長(zhǎng)期安全性隨訪等難題。
日本此次通過“條件承認(rèn)”制度為iPS療法打開了監(jiān)管之門,被國(guó)際媒體稱為“全球iPS療法走向社會(huì)化應(yīng)用的關(guān)鍵拐點(diǎn)”。接下來,業(yè)界關(guān)注的重點(diǎn)將聚焦于三件事:
- 正式批復(fù)的細(xì)節(jié):最終適用的具體適應(yīng)癥、患者人群界限以及嚴(yán)格的醫(yī)療機(jī)構(gòu)要求。
- 上市后評(píng)估方案:如何設(shè)定合理的終點(diǎn)指標(biāo)和評(píng)估頻率,以在7年內(nèi)完成證據(jù)鏈的閉環(huán)。
- 全球監(jiān)管的連鎖反應(yīng):日本先行一步后,這款產(chǎn)品將成為各國(guó)監(jiān)管機(jī)構(gòu)討論iPS細(xì)胞療法審批路徑的現(xiàn)實(shí)參照物,推動(dòng)該領(lǐng)域從“科學(xué)可行”全面進(jìn)入“制度可行”的新階段。
參考資料:
1.iPS Cell Products Win World-First Approval in Japan: Heart Failure and Parkinson’s Treatments Mark 20-Year Milestone
2.Big step toward world’s first practical use of iPS cells
免責(zé)說明:本文僅用于傳播科普知識(shí),分享行業(yè)觀點(diǎn),不構(gòu)成任何臨床診斷建議!杭吉干細(xì)胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請(qǐng)隨時(shí)聯(lián)系我。



 掃碼添加官方微信
掃碼添加官方微信